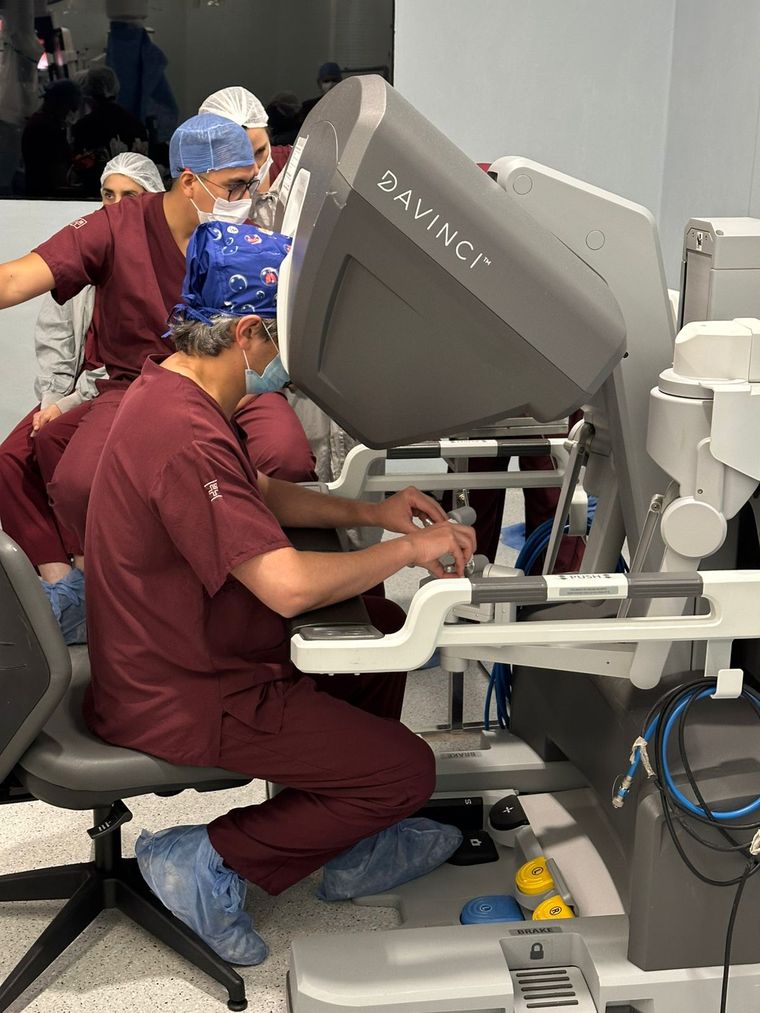
Los hospitales podrán importar equipos médicos usados y reacondicionados: cuáles son los requisitos
Una nueva normativa de la Anmat habilita a los hospitales, clínicas y centros de diagnóstico importar tecnología médica usada o reacondicionada.
Los hospitales podrán adquirir equipos médicos usados del exterior.
ShutterstockLa Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (Anmat) actualizó el régimen regulatorio para la importación de productos médicos usados y reacondicionados, con el objetivo de facilitar el acceso a tecnología sanitaria y optimizar los procesos administrativos.
La medida establece nuevas condiciones para el ingreso de equipamiento médico, diferenciadas según el nivel de riesgo y el estado de los dispositivos.
La normativa reemplaza regulaciones anteriores consideradas desactualizadas y permite que centros de salud públicos y privados, como hospitales, clínicas y centros de diagnóstico, puedan realizar directamente el trámite de importación. Hasta el momento, esta posibilidad estaba limitada a importadores y fabricantes.
La ampliación de los actores autorizados apunta a reducir costos y mejorar la capacidad de atención en instituciones sanitarias, especialmente en aquellas de menor escala.
-
Te puede interesar
Trigo: entre las buenas perspectivas climáticas y la presión de los costos
Cómo se llevará a cabo la importación de equipos médicos
El nuevo esquema define tres modalidades para importar productos médicos ya registrados ante la Anmat. La primera modalidad incluye equipos reacondicionados en el exterior, que deberán contar con la correspondiente certificación técnica. La segunda permite el ingreso de dispositivos usados que no requieren reacondicionamiento. En tanto, la tercera contempla el ingreso de equipos usados para ser reacondicionados dentro del país.
En todos los casos, la documentación requerida varía según el tipo de producto y su historial de uso.
Qué requisitos deben cumplir los equipos médicos importados
Los productos médicos deberán contar con certificados de reacondicionamiento o informes de verificación técnica emitidos por el fabricante, por servicios técnicos habilitados en el país o por entidades extranjeras radicadas en países con alta vigilancia sanitaria. En ese sentido, la Anmat especificó que los productos de uso único quedan excluidos de este régimen y tienen prohibida su importación bajo estas condiciones.
Para esto, la normativa introduce un sistema de control ajustado al nivel de riesgo de los dispositivos. Los productos considerados de bajo riesgo requerirán una intervención previa menor por parte del organismo regulador, lo que permitirá acortar los plazos para su ingreso al país. En cambio, los equipos de mayor complejidad seguirán estando sujetos a controles más estrictos y necesitarán una autorización expresa por parte de la Anmat antes de su importación.
En suma, el organismo explicó que esta actualización normativa responde a la necesidad de adaptar el régimen a los estándares internacionales y mejorar la disponibilidad de equipamiento médico en el sistema de salud argentino. Asimismo, la medida también busca facilitar la modernización tecnológica en instituciones que, por restricciones presupuestarias, encuentran dificultades para adquirir dispositivos nuevos.